A biotecnologia moderna mudou tudo. Nos últimos 50 anos, as novas tecnologias biológicas revolucionaram a área da saúde, transformando a forma como entendemos, diagnosticamos, tratamos e prevenimos doenças. Neste artigo exploramos a evolução da biotecnologia moderna em saúde no mundo e no Brasil, e apresentamos uma visão geral de desafios e perspectivas para o país.
Histórico da Biotecnologia Moderna
A manipulação de processos biológicos para obter novos produtos remonta a mais de 6.000 anos com o desenvolvimento inicial das técnicas de fermentação. No entanto, apesar das bases terem sido criadas antes, principalmente pela descoberta da estrutura da dupla hélice por Watson e Crick em 1953 e a identificação das enzimas de restrição pelas pesquisas de Werner Arber na década de 1960, foi entre a década de 1970 e 1980 que a verdadeira revolução ocorreu.
Em 1972, o cientista Paul Berg realizou o primeiro experimento de transferência de um gene de um ser vivo para outro. Isso seria a base para a tecnologia de DNA recombinante, permitindo isolar genes específicos humanos e inserí-los em microrganismos, que passaram então a produzir proteínas terapêuticas em larga escala. A insulina, indicada para o tratamento de diabetes, foi o primeiro produto biotecnológico lançado no mercado em 1982 pela empresa Eli Lilly.
Até o início da década de 1990, outros produtos seriam lançados. Em 1986, a Roche lançou o interferon alfa-2a, indicado para leucemia de células pilosas, abrindo caminho para o tratamento de diversos cânceres e doenças virais. No mesmo ano, a Schering-Plough (hoje Merck & Co.) lançou o interferon alfa-2b para a mesma indicação.
O ano seguinte marca o lançamento dos primeiros produtos por empresas puramente biotecnológicas. A Genentech (depois adquirida pela Roche) lançou o hormônio do crescimento humano recombinante, permitindo o tratamento da deficiência do hormônio com um produto seguro e eficaz. E a Amgen, colocou no mercado a eritropoetina, indicada para anemia associada à insuficiência renal crônica, revolucionando o tratamento da anemia em pacientes renais, reduzindo a necessidade de transfusões de sangue.
Em 1990, a Amgen lançou seu segundo produto no mercado, o fator estimulador de colônias de granulócitos (G-CSF), para a prevenção de neutropenia febril em pacientes submetidos a quimioterapia. O produto reduziu significativamente o risco de infecções em pacientes com câncer submetidos à quimioterapia.
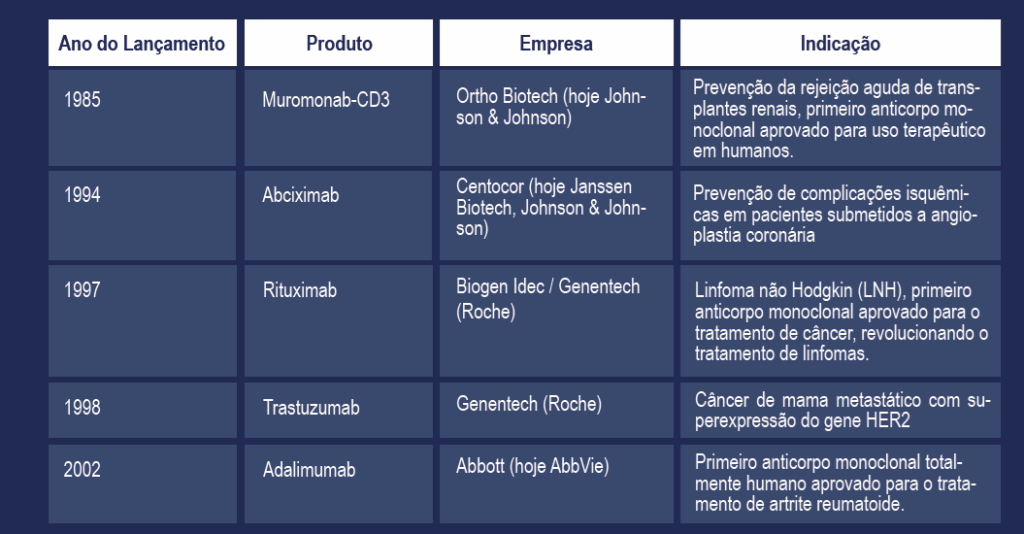
Na mesma época, começaram a surgir no mercado farmacêutico os primeiros anticorpos monoclonais, abrindo caminho para terapias direcionadas, capazes de reconhecer e atacar células específicas, como as células cancerosas.Quase ao mesmo tempo, a área de diagnósticos desenvolvia tecnologias de forma gradual, em escala laboratorial, antes de serem comercializados em larga escala, como radioimunoensaio, ELISA, southern-blot e Hibridização In Situ Fluorescente (FISH).
Quase ao mesmo tempo, a área de diagnósticos desenvolvia tecnologias de forma gradual, em escala laboratorial, antes de serem comercializados em larga escala, como radioimunoensaio, ELISA, southern-blot e Hibridização In Situ Fluorescente (FISH).
Entretanto, foi na década de 1990 que ocorreu a grande revolução do diagnóstico molecular com o lançamento de duas tecnologias principais. A Reação em Cadeia da Polimerase (PCR) começou a ser utilizada para amplificar o material genético de patógenos (vírus, bactérias, fungos) em amostras clínicas, permitindo o diagnóstico de doenças infecciosas, como HIV, hepatite C, tuberculose e clamídia. Em seguida, os testes de DNA para identificação genética e forense, utilizando marcadores genéticos (STRs, SNPs) para identificar indivíduos e determinar relações de parentesco.
As décadas de 2010 e 2020 foram marcadas por avanços na genômica e na imunoterapia, que abriram novas perspectivas para o tratamento de doenças complexas. Tecnologias biológicas como o sequenciamento de DNA, a imunoterapia e a edição genética abriram uma nova frente de crescimento e capacidade de tratamento de doenças complexas.
O sequenciamento do genoma humano permitiu o diagnóstico de doenças genéticas, em testes neonatais para doenças como fibrose cística, fenilcetonúria e hipotireoidismo congênito, de doenças raras, permitindo o diagnóstico preciso e acesso a tratamentos, em geral, conjugados e o aconselhamento de doenças genéticas, possibilitando um melhor planejamento familiar. A tendência atual, com a redução dos custos, é ampliar o alcance da medicina personalizada, como já vem acontecendo em em especial em oncologia.
A imunoterapia, que estimula o sistema imunológico a combater o câncer, revolucionou o tratamento de diversos tipos de tumores. Tratamentos com inibidores de checkpoint (PD-1, CTLA-4) e terapias celulares (CAR-T) tem demonstrado melhora significativa na sobrevida de pacientes com melanoma metastático, câncer de pulmão, linfoma de Hodgkin e outros tipos de câncer, chegando a atingir a remissão completa em alguns casos. Além disso, anticorpos monoclonais e outras terapias biológicas que modulam o sistema imunológico são usados para tratar doenças autoimunes como artrite reumatoide, doença de Crohn, esclerose múltipla e psoríase.
As tecnologias de edição genética, muitas ainda em desenvolvimento e estudos clínicos, serão capazes de impactar o tratamento de doenças hereditárias, vários tipos de cânceres e doenças infecciosas. As aplicações já disponíveis para distúrbios como anemia falciforme, atrofia muscular espinhal (AME) e leucemia linfoblástica aguda (LLA) apontam para o papel que a edição genética terá no futuro, representando uma nova fronteira na medicina.
Impactos da Biotecnologia Moderna

O impacto da biotecnologia moderna na saúde é inegável. A biotecnologia tem tido um papel significativo no aumento da qualidade e expectativa de vida da população no mundo. Os pacientes com doenças crônicas têm tido suas condições controladas, permitindo uma vida saudável e produtiva.
Os medicamentos biológicos, como imunoterápicos e terapias-alvo, se provaram eficazes e seguros para o aumento da sobrevida e tratamento de doenças antes consideradas incuráveis, como diversos tipos de cânceres e doenças autoimunes e genéticas. Os medicamentos retrovirais transformaram a AIDS de uma doença fatal em uma condição crônica controlável.
E as novas vacinas têm provocado uma redução significativa da mortalidade infantil. A erradicação de doenças como poliomielite se tornaram possíveis em muitos países.
Além disso, a biotecnologia moderna permitiu o desenvolvimento de testes de diagnóstico molecular, que são mais rápidos, precisos e sensíveis do que os testes tradicionais para detectar doenças infecciosas, câncer e doenças genéticas. As tecnologias já possibilitam um diagnóstico cada vez mais precoce e específico, utilizando informações genéticas para adaptar o tratamento de cada paciente.
A biotecnologia abriu ainda caminho para as terapias gênicas, através de tecnologias como CRISPR-Cas9, que oferecem a possibilidade de inserir, remover ou alterar sequências específicas de DNA defeituosos e, assim, curar doenças genéticas e cânceres.
O Cenário Brasileiro
A presença dos biológicos no mercado nacional, como no restante do mundo, é relevante. O mercado de medicamentos biológicos cresce no Brasil e no mundo a uma taxa de quase 15% ao ano e já representa cerca de 30% do mercado farmacêutico total no país. No mundo, o percentual de participação dos biológicos vem crescendo nas últimas décadas, de menos de 10% no ano 2000 para uma estimativa superior a 40% em 2025.
O Brasil tem investido no desenvolvimento da biotecnologia em saúde, com o objetivo de fortalecer a produção nacional de biofármacos e reduzir a dependência de importações. Desde 2010, produtos biológicos aparecem na lista de produtos estratégicos do Sistema Único de Saúde (SUS), o que possibilita a estruturação de projetos dentro do programa de Parcerias para o Desenvolvimento Produtivo (PDPs) do Ministério da Saúde.
Além disso, desde 2013, instituições como a Financiadora de Estudos e Projetos (FINEP) e o Banco Nacional de Desenvolvimento Econômico e Social (BNDES) têm apoiado, com recursos de subvenção, financiamento e investimento direto, os projetos de inovação no mercado biotecnológico.
Do ponto de vista regulatório, tem havido significativos avanços. Como exemplo, em 2010, o país, de forma pioneira na América Latina, criou uma legislação específica para os biossimilares a fim de aumentar a discussão e necessidade deles no sistema de saúde.
Neste cenário, grandes empresas farmacêuticas locais, laboratórios oficiais, liderados por Fiocruz e Butantan, e biofarmacêuticas nacionais, como Bionovis e Biomm, vem crescendo de forma significativa, embora ainda longe dos padrões internacionais, seus investimentos em projetos de medicamentos biológicos.
O país conta com um crescente ecossistema de inovação, constituído por startups promissoras, universidades e centros de pesquisa que atuam na pesquisa e desenvolvimento de novos produtos e processos. Biotechs locais enfrentam o desafio de avançar seus projetos pelas fases pré-clínica e clínica, ao mesmo tempo em que as infraestruturas são também criadas, e um emergente ambiente de investimento de capital se estrutura.
Desafios e Perspectivas

No ambiente global, a biotecnologia ainda enfrenta desafios. As novas biotecnologias exigem processos complexos de manipulação celular, altos investimentos em infraestrutura, pessoal altamente qualificado e processos de controle de qualidade rigorosos para atender as exigentes normas regulatórias nos principais mercados.
Neste cenário, os custos de desenvolvimento de um novo fármaco crescem e precisam ser repassados aos preços. Com produtos mais específicos, os volumes caem e pressionam ainda mais os preços aos pacientes e aos sistemas de saúde. O alto custo dos medicamentos biológicos limita o acesso a tratamentos mais eficazes e amplia as desigualdades sociais.
Apesar dos avanços, o setor de biotecnologia no Brasil ainda enfrenta desafios, como o baixo investimento em pesquisa e desenvolvimento, a carência de infraestruturas adequadas na cadeia de desenvolvimento de produtos, desafios regulatórios e a dependência de importações de insumos. No entanto, o país tem potencial para se tornar um importante player no mercado global de biofármacos, impulsionado pelo seu sistema de saúde universal, pela sua biodiversidade e pela sua capacidade de inovação.
Ao longo de sua história, a Biominas tem tido envolvimento em iniciativas e atividades que possam contribuir para o crescimento do ambiente de inovação em tecnologias biológicas para a saúde e para o posicionamento do país como player relevante no setor. Com especial atenção, temos focado nosso trabalho na solução de 3 grandes gargalos atuais:
- Infraestrutura
É necessário que recursos, tanto públicos quanto privados, sejam direcionados à construção e operação de infraestrutura, tanto para desenvolvimento quanto para validação de novas tecnologias. No acompanhamento de startups inovadoras, muitas delas deep techs, identificamos uma primeira barreira clara: a escassez de estrutura validada para ensaios não-clínicos e pré-clínicos. O país carece de prestadores de serviço na área que sejam capazes de entregar soluções a um nível de qualidade global.
Uma segunda barreira na validação de tecnologias inovadoras é a produção de lotes piloto. O país não dispõe de estruturas validadas internacionalmente de Contract Development and Manufacturing Organization (CDMO) para dar vazão ao número de projetos em desenvolvimento.
- Pesquisa Clínica
Desde a pandemia de Covid-19, o Brasil tem se destacado mais no cenário global de pesquisa clínica. Apesar de notarmos um aumento da demanda por centros de pesquisa clínica e CROs brasileiras, ainda compomos apenas cerca de 2% dos ensaios clínicos globais realizados no mundo. O Brasil possui aspectos atrativos para a condução de ensaios clínicos, mas é preciso uma profissionalização de centros e profissionais para atingir em escala o potencial do país.
- Capacitação Profissional
Os dois primeiros desafios passam pela capacitação profissional. O Brasil possui excelentes centros de pesquisa e acadêmicos renomados em todo o mundo. Contudo ainda precisamos percorrer um grande caminho na profissionalização de profissionais científicos para o setor produtivo. Para obter sucesso, seja no surgimento de novas tecnologias e startups, e na prestação de serviço especializada, precisamos de profissionais que atendam a critérios globais de qualidade. Para além da mão de obra capacitada para os desafios de hoje, precisamos também nos preparar para o futuro, com profissionais que façam a integração entre biologia, biotecnologia e inteligência artificial, colocando o Brasil na fronteira da ciência.
Esses desafios são vistos em todo o mundo, apesar de em escalas diferentes. Alguns países também considerados em desenvolvimento já saíram na frente do Brasil nos últimos 10 a 20 anos, como é o caso da Índia, China e Coreia do Sul. Contudo, as mudanças econômicas e políticas no mundo e as novas fronteiras tecnológicas trazidas pela inteligência artificial, mudam as perspectivas de crescimento econômico para todo o mundo, e o Brasil precisa se estabelecer, a partir dos seus ativos estratégicos, como um player importante no mercado global.
As terapias avançadas, como a terapia gênica e a terapia celular, representam uma nova fronteira para a biotecnologia em saúde. Vemos no Brasil empresas e startups com capacidade de desenvolvimento de tais tecnologias, mas os desafios citados acima continuam sendo um problema para seu escalonamento a nível global. É necessário segurança jurídica e regulatória, somada a infraestrutura e mão de obra qualificada, para garantir investimentos de padrões globais, para que posteriormente o Brasil se torne exportador de tais tecnologias. Dessa forma, poderemos competir com os países líderes deste setor.
Além disso, a crescente digitalização da saúde, com o uso de tecnologias como big data e inteligência artificial, oferece novas oportunidades de integração tecnológica para o desenvolvimento de terapias mais personalizadas e eficazes, sendo essa a nova fronteira para todo o mundo
Na soma de velhos desafios e os novos desafios, o Estado brasileiro e nossas instituições, sejam elas privadas ou públicas, precisam desenhar e executar um plano estratégico do setor que ditará como será o cenário das tecnologias biológicas no país nos próximos 35 anos.





