
Uma nova ferramenta de edição genética capaz de mudar completamente o mundo que conhecemos cada vez mais perde o rótulo de promessa e ganha o de “realidade”.
O nome da técnica é Crispr-Cas9 (lê-se crísper-cás-nove) e ela reúne características que surpreendem até mesmo os biologistas mais experientes e está para o genoma assim como um processador de texto está para as palavras e frases de uma redação.
Simplificadamente, agora é possível eliminar partes indesejadas do genoma –que causam doenças– e, se necessário, inserir novas sequências no local.
A taxa de sucesso, quantidade de células modificadas pela técnica, é muito maior que aquela de outras antigas, usadas em experimentos de terapia gênica, por exemplo.
Antes, eram oferecidos genes inteiros para células doentes na esperança de que elas os acolhessem e os incorporassem. A maquinaria de edição do Crispr permite atuar diretamente no gene defeituoso, como um míssil teleguiado, atingindo um grande número de células-alvo.
Na técnica, a enzima Cas9, uma nuclease, corta as duas fitas da dupla hélice do DNA, abrindo espaço para a inserção, se for o caso, de um novo trecho (veja infográfico). Agora também é possível uma edição “sem corte” do DNA –útil para alterar uma única “letra” do genoma.
A novidade está na última edição da revista “Nature”. Mutações de uma única “letra” causam doenças como anemia falciforme e aumentam propensão a alguns cânceres.
No caso da distrofia muscular de Duchenne, doença progressiva e letal, a técnica poderia beneficiar 80% dos pacientes, ao cortar fora um trecho “errado” do DNA das células musculares.
As possibilidades são infinitas. Recentemente, cientistas mostraram, usando o Crispr, ser possível “empurrar” mosquitos vetores de doenças (como o anopheles, da malária e o aedes, da dengue e da zika) rumo à extinção ao favorecer a herança de genes letais entre as fêmeas. Outro exemplo icônico é experimento que extirpou o HIV de uma cultura de células humanas.
Para entender o possível impacto do Crispr e de outras futuras técnicas de manipulação genética, tem de se ter em mente que humanos, vacinas, agropecuária, vacinas –todo o mundo vivo ou que depende dele– estão na mira.
Células embrionárias podem ser modificadas para um bebê não ter fibrose cística, distrofia ou propensão ao diabetes e à obesidade.
Bactérias capazes de degradar de poluentes, como óleo, podem ser aperfeiçoadas. Plantas com altíssima capacidade de sequestro de carbono (capazes de atenuar o aquecimento global) podem estar logo ali, alguns anos adiante.
Com relação à saúde, não é uma técnica que apenas eliminaria uma bactéria ou vírus, mas que teria potencial de arrumar tudo o que está “errado” na célula. Saber o que é “errado” envolve uma grande discussão bioética, porém.
Cientistas de várias partes do mundo estão em uma espécie de corrida armamentista para ver quem consegue ir mais longe com o Crispr. Uma preocupação é quando o primeiro bebê-Crispr nascerá. Houve até proposta de “trégua” na área, da cientista Jennifer Doudna, da Universidade da Califórnia, em Berkeley.
A ideia de Doudna seria a de que houvesse diretrizes, ou, ao menos, um “guia de boas práticas” para quem estivesse usando a ferramenta em células embrionárias humanas. No Reino Unido, por exemplo, já há pesquisas com embriões humanos com a finalidade de melhorar o desempenho da reprodução assistida.
DINHEIRO
O Crispr não é uma invenção humana e o acrônimo significa “repetições palindrômicas curtas agrupadas e regularmente interespaçadas”. Originalmente, trata-se de um recurso utilizado por organismos unicelulares contra a invasão de vírus. A transformação desse conhecimento em técnica genética só ganhou importância no início desta década.
Doudner e sua colega Emmanuelle Charpentier iniciaram o processo de patenteamento em 2013, pouco antes de Feng Zhang, do Instituto de Tecnologia de Massachussets (MIT) fazer o mesmo por uma via menos burocrática.
Zhang teve sucesso, e iniciou-se uma disputa institucional e pessoal para ver quem é o dono do Crispr. Dada a gama de possíveis aplicações, o potencial de exploração econômico da técnica é incalculável. O mundo ainda aguarda a decisão da justiça americana.
Por ora, já existem empresas explorando o potencial do Crispr e engordando a conta de Zhang. Só neste mês de abril, a Intella Therapeutics, joint venture da qual participa a farmacêutica Novartis, deve captar quase US$ 120 milhões em investimentos. Outra empresa, a Editas Medicine, levantou US$ 94 milhões em sua oferta pública inicial.
Mesmo com a briga judicial, provavelmente o risco do negócio vale a pena.
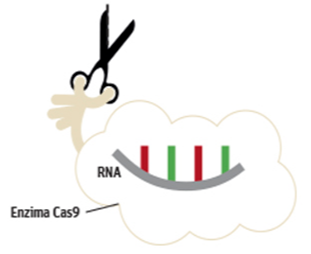
A TÉCNICA A enzima Cas9 serve como “tesoura molecular”. Ela carrega uma fita de RNA dentro dela. O RNA ajuda a encontrar o trecho de DNA a ser editado.
A enzima Cas9 serve como “tesoura molecular”. Ela carrega uma fita de RNA dentro dela. O RNA ajuda a encontrar o trecho de DNA a ser editado.
O CORTE
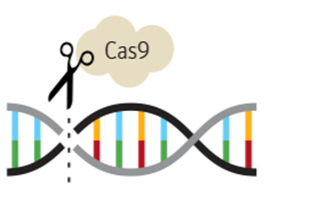 Quando o alvo é identificado, a enzima Cas9 corta o DNA em dois, impedindo a replicação de um vírus ou, no caso da técnica de edição, alterando a sequência de um genoma.
Quando o alvo é identificado, a enzima Cas9 corta o DNA em dois, impedindo a replicação de um vírus ou, no caso da técnica de edição, alterando a sequência de um genoma.
CORREÇÃO
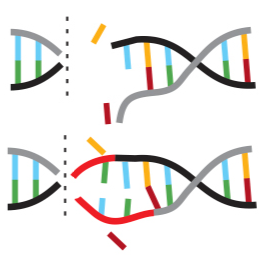 Após o corte, o DNA tenta se regenerar, sofrendo alterações em sua sequência. O gene pode ser ‘desativado’ no processo.
Após o corte, o DNA tenta se regenerar, sofrendo alterações em sua sequência. O gene pode ser ‘desativado’ no processo.
COLAGEM
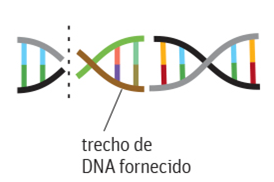
Novos trechos do DNA, se oferecidos à célula, permitem maior controle sobre o processo de edição do genoma, customizando sua função.
EXEMPLOS
Um dos casos de sucesso já reportados pelos cientistas envolve o reparo de proteínas importantes para a contração do músculo, melhorando a distrofia muscular; em outro caso, alterou-se o DNA de mosquitos, reduzindo a transmissão de malária
Fonte: Portal Folha de São Paulo
Ainda não recebemos comentários. Seja o primeiro a deixar sua opinião.





Deixe um comentário